挚盟医药创立于2018年,是一家临床阶段专注于肝病和神经/精神系统疾病领域原创小分子药物研发的公司。作为一家专注于肝病领域的创新药研发平台,挚盟的产品管线涵盖乙型肝炎病毒治疗的多个环节,包括抑制病毒复制的核衣壳组装调节剂、免疫调节剂、以及抑制乙肝病毒表面抗原的RNA去稳定剂。公司希望通过多方位抑制病毒的复制和病毒蛋白的表达,同时诱导有效的抗病毒免疫应答来抑制病毒,最终实现慢性乙型肝炎的功能性治愈。除了在慢性乙型肝炎功能性治愈领域的布局,挚盟医药还深度布局了难治性癫痫、神经性疼痛(如癌性疼痛)、渐冻症、抑郁症、双向情感障碍等神经系统疾病的创新药研发。目前公司已经有多个产品进入了临床阶段。
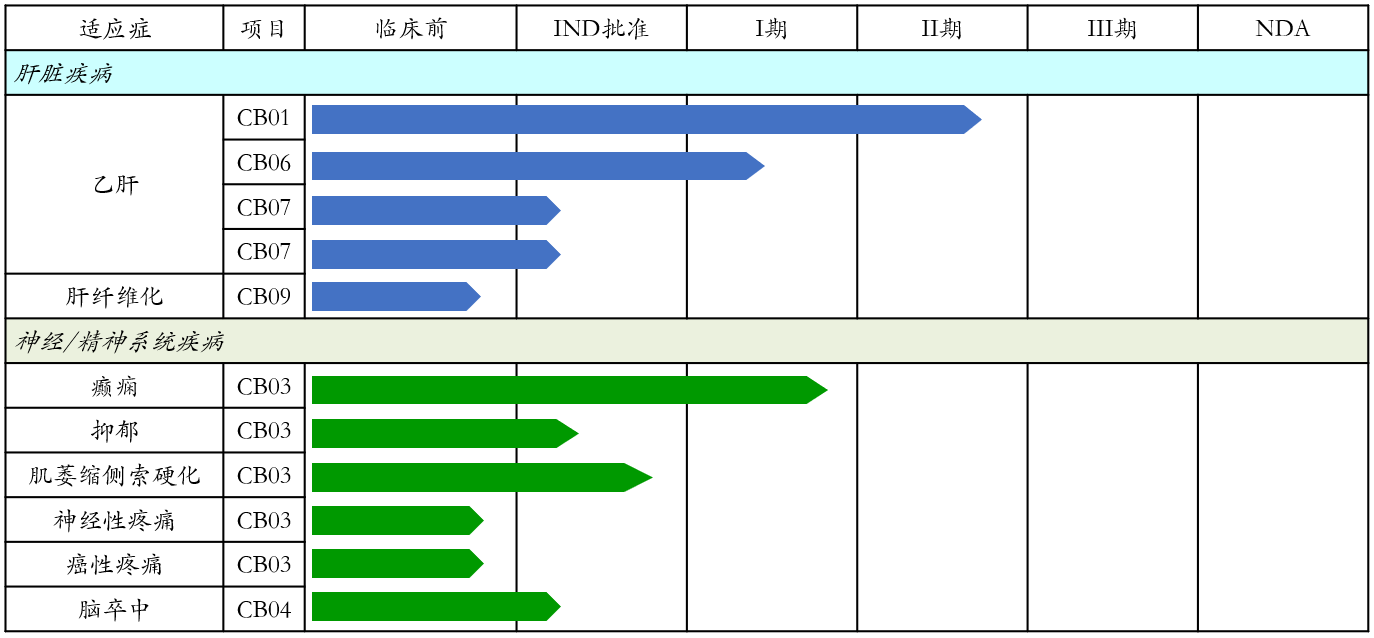
慢性乙肝药物研究
据相关资料显示:中国的乙型肝炎病毒(HBV)携带者约为8600万,其中约有3000万人为慢性乙型肝炎患者(CHB), 但诊断率仅18.7%,治疗率不足11%,远低于WHO 2030年目标(诊断率90%、治疗率80%)。在中国,超过80%的肝癌(HCC)病例归因于慢性HBV感染。虽然目前的核苷类抗病毒药物可有效控制大部分病人的HBV复制并延缓肝硬化的进展,但还有很大比例的病人不应答或应答不完全,另外它们很少可以治愈慢性乙肝,患者需要长期用药以及面临停药后病毒反弹的可能性,因此,迫切需要针对HBV生命周期不同阶段的新型治疗方案。
针对肝脏疾病病因的复杂性,挚盟采用的策略是研发多种新颖且有效的直接抗乙型肝炎病毒(HBV)药物,对HBV的生命周期进行多阶段性和多方位的抑制;然后,通过使用新型免疫调节剂恢复患者的免疫功能,最大限度地抑制HBV cccDNA 活性和清除病毒感染的细胞。我们的目标是为慢性乙肝患者的治愈,研发更加有效、安全和负担得起的创新药物,以满足患者急切的临床需求、改善患者的生命质量。
HBV核衣壳抑制剂 (ZM-H1505R)
乙型肝炎病毒(Hepatitis B Virus,HBV)核心蛋白(Core protein)在HBV的生命周期具有重要的作用。在HBV感染肝细胞后,Core蛋白以二聚体的形式表达在肝细胞内,可与HBV前基因组RNA/聚合酶复合物组装形成核衣壳(Capsid)。在Capsid内,病毒完成逆转录,并形成双链DNA基因组。开发通过干扰Core蛋白的功能来阻断HBV复制的药物,是当前直接抗病毒药物研发的热点。
核衣壳组装调节剂(Capsid Assembly Modulator,CAM)能作用在Core蛋白二聚体间的疏水口袋中,影响Capsid的组装和解聚。一方面CAM能干扰正常Capsid的组装过程,抑制病毒复制,减少慢性HBV感染者外周血中的病毒标志物,另一方面CAM能抑制新发感染(de novo infection)过程和细胞内复制过程中Capsid的解聚,阻断HBV再感染的过程,降低肝脏内的总病毒负荷。
挚盟医药自主研发的核衣壳组装调节剂ZM-H1505R是一种II型CAM分子,不同于其它在研的I型和II型HBV核心蛋白变构调节剂,它是一款全新的吡唑类化学结构,通过影响Core蛋白组装Capsid的过程,诱导形成不具有复制活性的、空的Capsid,从而阻断HBV的复制过程。在较高浓度的条件下,ZM-H1505R还能够抑制HBV的新发感染过程,减少HBV共价闭合环形DNA(covalently closed circular DNA,cccDNA)的形成。cccDNA是病毒转录的模板,以微小染色体的形式存在于肝细胞核内。由于目前已经获批上市的HBV治疗药物缺乏有效清除cccDNA的机制,稳定存在的cccDNA是HBV能发生持续性感染并无法达到功能性治愈的最重要的原因之一。与此同时,ZM-H1505R具有良好的肝靶向特征。
ZM-H1505R在II期临床试验中显示可迅速使已经接受长期(如,一年以上)NAs治疗但未达到完全应答的 LLV慢乙肝病人HBV DNA下降至检测水平以下,达到完全病毒学应答(血浆HBV DNA定量检测值≤10 IU/mL)。并且II期结果表明ZM-H1505R具有优异的安全性和耐受性。2025年1月,ZM-H1505R片被CDE认定为突破性治疗药物,针对适应症为慢性乙型肝炎的治疗。
TLR8激动剂 (CB06-036)
CB06-036是上海挚盟医药科技有限公司自主研发的一款小分子口服TLR8激动剂,拟用于治疗慢性乙型肝炎病毒感染。
TLR8的全称为Toll样受体8 ,它可识别病原体衍生的单链RNA片段,以触发先天性和适应性免疫反应。研究发现,慢性乙型肝炎与功能失调的免疫反应有关,因此选择性TLR8激动剂被认为可能是一种有效的治疗选择。
在临床前研究中,CB06-036表现出了良好的选择性、活性及安全性,可以在人外周血单核细胞中诱导细胞因子,这些细胞因子能够通过多种免疫介质激活抗病毒功能。与此同时,CB06-036具有良好的肝靶向特征。
2022年4月, TLR8激动剂CB06-036在美国完成1期临床试验首次健康受试者用药。这是一项随机、双盲和安慰剂对照的1期临床研究,目的是评估CB06-036单次递增剂量在健康成人受试者中的安全性、药代动力学和药效学。2025年6月,CB06-036在中国和新西兰完成了在慢性乙肝患者中的1b期临床试验。
2022年11月,挚盟医药与葛兰素史克(GSK)就TLR8激动剂CB06-036达成全球独家许可协议。挚盟医药在成功完成1期临床研究后,将允许GSK开发、生产和商业化CB06-036。如果获得成功,CB06-036可以作为联合用药或与bepirovirsen进行序贯治疗,有可能为更多乙肝患者提供功能性治愈。
神经/精神系统疾病药物研究
KCNQ2/3钾离子通道开放剂 (CB03-154)
CB03-154是由挚盟医药自主开发的一种钾离子通道KCNQ2/3 开放剂,用于治疗难治性癫痫、成人肌萎缩侧索硬化症(ALS)、抑郁症和双向情感障碍等患者。
癫痫是最常见的神经系统疾病之一,其特征是癫痫发作或阵发的异常行为、感觉,有时甚至丧失意识,影响全球约9000万人,中国患者为900万左右。癫痫患者的管理有三个目标:控制癫痫发作、避免治疗期间的不良反应和恢复生活质量。虽然药物治疗能有效控制大多数癫痫病例的发作,但远未满足癫痫患者临床需求---约30%的癫痫患者为单药无法控制的难治性癫痫。瑞替加滨(Potiga,Ezogabine,Retigabine)是2011年FDA和EMA批准的第一个KCNQ2/3钾离子通道开放剂,用于其它药物无效的难治性癫痫的治疗;但由于色素沉着导致的视力受损风险,瑞替加滨于2017年退出市场。挚盟医药的CB03-154是新一代KCNQ2/3钾离子通道开放剂,与瑞替加滨相比,CB03-154具有更好的化学和代谢稳定性、更好的选择性和抗癫痫活性、更好的药动学性质及安全性。
肌萎缩侧索硬化(ALS)是一种严重的致残和致死性的神经系统变性/退行性疾病,患者进行性地发生骨骼肌无力、萎缩,进而累及呼吸运动系统发生呼吸衰竭而死亡,中位生存期通常为出现症状后2-3年。由于该疾病的病因和发病机制尚未完全明确,因此目前治疗手段极其有限。目前全球只有四种ALS治疗药物被批准用于延缓ALS病情发展。但现有的ALS治疗只能起到小幅改善患者功能或轻微延长生存期的作用,尚无可以阻止或逆转疾病进展的治疗方法,ALS患者仍然存在巨大的未满足的临床治疗需求。
研究证实,运动神经元过度兴奋是ALS的重要病理生理过程,早期识别和调节过度兴奋的运动神经元可以形成神经元保护作用。第一个上市的ALS治疗药物利鲁唑即通过降低神经元兴奋性而具有延长患者生存期的作用,但是延缓疾病进程的作用有限。研究显示ALS患者中运动神经元的过度兴奋与 Kv7.2/7.3(KCNQ2/3) 活性降低有关,第一代Kv7.2/7.3(KCNQ2/3) 开放剂瑞替加滨(RTG/EZG)经研究证实可以降低ALS患者运动神经元的过度兴奋,具有延缓运动神经元变性、提高存活能力的潜在治疗作用。
CB03-154是由挚盟医药开发在研的最新一代钾离子通道2/3( Kv7.2/7.3 或 KCNQ2/3 )开放剂,拥有本品的自主知识产权,临床前研究已证实CB03-154可显著降低ALS运动神经元的过度兴奋,显著减缓与肌肉力量相关的功能参数的恶化,延迟发病,延长生存期并使肌肉和神经元形态正常化。CB03-154不仅具有改善ALS患者神经退行性病变的相关症状的作用,而且有延缓病程进展等潜在临床治疗价值。2023年,CB03-154获得FDA的ALS孤儿药认证。公司拟首先在中国开展治疗ALS的临床研究。